Mida me teame Venemaa esimesest koroonaviiruse ravimist
Tervis / / December 29, 2020

N + 1 - populaarteadus väljaanne teaduses, inseneriteaduses ja tehnoloogias praegu toimuvast.
Esimene Venemaa koroonaviiruse ravim "Avifavir" sai tervishoiuministeeriumilt heakskiidu. Ravimi arendaja lubab, et saadab esimesed ravimipartiid haiglatesse 11. juunil. Me saame aru, kust need kollased pillid tulid, kuidas ravim toimib, milline kliiniline ta on testid juba läbinud ja kas on võimalik kindlalt öelda, et meil on ravim COVID-19.
Kust see tuli
Avifaviir on Venemaa ravimi kaubanimi, mille on välja töötanud Venemaa otseinvesteeringute fond (RDIF) ja ettevõtete grupp ChemRar. Ravimi toimeainet ei leiutatud Venemaal.
Selle rahvusvaheline mittekaubanduslik nimetus on favipiraviir. Välja töötanud Jaapani ettevõtte Toyama Chemical töötajadToyama Chemical Co Ltd - FUJIFILM Pharmaceuticals Corporationi tütarettevõte.
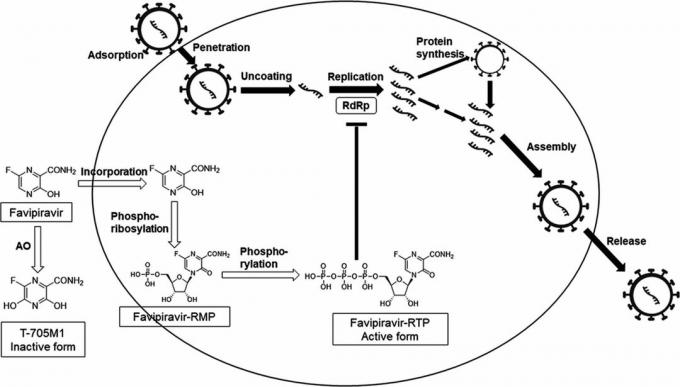
Keemilise struktuuri järgi on favipiraviir derivaatFavipiraviir 6 - fluoro - 3 - okso - 3,4 - dihüdropürasiin - 2 - karboksüülhape või pürasiinkarboksamiid. Keemiaraamatukogu sõeluuringu käigus avastasid Toyama töötajad, et sellel ainel võib olla gripiviiruse vastane toime: viirusega nakatunud rakkudes muundatakse favipiraviir aktiveeritud vormiks, mis pärsib olulise viirusensüümi, RNA-sõltuva RNA-polümeraasi, aktiivsust
Koroonaviiruse haigus 2019 (COVID-19): haiglaravil viibivate täiskasvanute ravi.Kui RNA polümeraas on välja lülitatud, kaotavad gripiviirused võime oma geneetilist materjali RNA nakatunud rakkudesse printida. Seetõttu peatub juba rakkudesse sisenenud viiruse tootmine. See on ravimi ainulaadsus - tavaliselt võivad viirusevastased ravimid takistada viiruste sisenemist rakkudesse.
RNA-sõltuvat RNA-polümeraasi ei leidu ainult viirustes gripp, aga ka kõigis RNA viirustes. Pealegi on RNA polümeraasi katalüütiline domeen - see on selle molekuli osa nimi, tänu millele ensüüm põhimõtteliselt saab töötada - on kõigis RNA viirustes ühtemoodi üles ehitatud. Kuna favipiraviir seondub täpselt RNA polümeraasi katalüütilise domeeniga, oli jaapanlastel põhjust seda ainet pidada laia levikuga viirusevastaseks aineksFavipiraviir (T - 705), viirusliku RNA polümeraasi laia toimespektriga inhibiitor toimespekter.
Toyama töötajad registreerisid favipiraviiri kaubanime Avigan all ja hakkasid uurima paljulubava ravimi aktiivsust RNA viiruste suhtesFavipiraviir (T - 705), uudne viirusliku RNA polümeraasi inhibiitor: A- ja B-tüüpi gripiviirustest Ebola viirusteni. Tulemused olid erinevad. Näiteks Ebola viiruse puhul selgus, et see ravim toimis ahvidelFavipiraviiri viirusevastane efektiivsus Ebola viiruse vastu: translatiivne uuring Cynomolgus macaques'iga, kuid inimestele rakendatuna on tulemusElulemus paranes favipiraviiriga ravitud Ebola patsientidel ei olnud eriti muljetavaldav. Ühest küljest oli 73 favipiraviiriga ravitud Guinea patsiendi suremus madalam kui patsientidel, kes olid proovinud tervendada muul viisil. Teisest küljest ei olnud erinevus nii suur: 42,5 protsenti versus 57,8 protsenti - see on võimatu veenduge, et see pole ainult juhuslik loendamine, mis on seotud asjaoluga, et patsientide valim oli väga suur väike. Sellele vaatamata kiitis Guinea valitsus heaksJaapan saatis Fujifilmi gripiravimi favipiraviiri Covid-19 uuringuteks enam kui 40 riiki seda ravimit kasutatakse Ebola viiruse standardravina.
Ravimi kodumaal Jaapanis õnnestus Aviganil Registreeri alles 2014. aastal - ja ainult uute gripiviiruse tüvede vastu. Aviganit ei ole kasutatud hooajalise gripi vastu.

Pealegi ei olnud ravim heaks kiidetud mitte ainult "uue" gripi vastu, vaid eranditult olukordades, kus olemasolevad viirusevastased ravimid olid ebaefektiivsed - st viimase abinõuna. Kuue aasta jooksul alates heakskiitmise hetkest pole sellist olukorda tekkinud kordagi, nii et tõelise gripiepideemia tingimustes ei kasutatud seda ravimit kunagi.
Ülevaade 29 kliinilisest uuringust (4299 osalejat), millest kuus olid 2. ja 3. faasi uuringud (juba hinnatakse) ravimi efektiivsus) näitas, et favipiraviiril "on soodne ohutusprofiil": tõsiste kõrvaltoimete osakaal välja mõeldudFavipiraviiri ohutuse ülevaade - potentsiaalne ravi COVID-19 pandeemias? 0,4 protsenti. Ikka turvalisuse probleemid ravim ikka jäävad.
Rõhutasid Jaapani teadlased, kes uurivad ravimi kasutamist raske gripi korralFavipiraviir, gripivastane ravim eluohtlike RNA viirusnakkuste vastuet Avigan on rasedatele vastunäidustatud: ravimil oli loomadele teratogeenne ja embrüotoksiline toime. Muud võimalikud probleemidFavipiraviir (Ameerika Ühendriigid: pole kaubanduslikult saadaval; vt Ravimi väljakirjutamise ja juurdepääsupiirangud): teave ravimiteabe kohta: söögiisu vähenemine, iiveldus, oksendamine, kusihappe kontsentratsiooni tõus veres (hüperurikeemia) ja maksakahjustus.
Praegu loen🔥
- Koronaviiruse tagajärjed võivad olla eluaegsed. Siin on sellest teada
Favipiraviir ja COVID-19
2020. aasta märtsis ütles Hiina tervishoiuministeeriumi koosseisu kuuluva riikliku biotehnoloogia arenduskeskuse direktor Zhang Xinmin.Favipiraviir näitab COVID-19 ravis head kliinilist efektiivsust: ametliket favipiraviir "on näidanud head kliinilist efektiivsust uudse koronaviirushaiguse (COVID-19) vastu". Andmete järgiCOVID - 19 eksperimentaalne ravi favipiraviiriga: avatud märgistusega kontrolluuring vähemalt ühes avatud, randomiseerimata uuringus osales 35 koronaviirushaigusega Hiina patsienti, kes said favipiraviiri (uuringus ei öeldud millist ravimit arutati - originaal Avigan või sama toimeainega Hiina ravim), paranes kiiremini ja kannatas vähem tüsistuste all kui 45 patsiendidkeda raviti teiste ravimitega (lopinaviir ja ritonaviir).
Praegu hinnatakse ravimi efektiivsust COVID-19 vastuKoroonaviiruse haigus 2019 (COVID-19): haiglaravil viibivate täiskasvanute ravi kliinilistes uuringutes Jaapanis. 9. aprill teatas FUJIFILMFujifilm teatas oma gripi viirusevastase ravimi "Avigan® tablett" II faasi kliinilise uuringu algusest COVID-19 patsientidele USA-s. Ameerika Ühendriikides toimuvate Avigani kliiniliste uuringute teise etapi alguses osaleb uuringus 50 koronaviirushaigusega patsienti. Mõnede välismaiste andmete kohaselt testiti favipiraviiri aprillis-mais veel 16 kliinilises uuringus, kuid mitte üheski lõpetatud kliiniline uuring, mis näitab, et favipiraviir või Avigan on efektiivsed koronaviiruse vastu haigus, ei.
Vene narkootikum
Iga ravim koosneb toimeainest ja täiteainest (valmis ravimvorm). Vene viirusevastane ravim sisaldab sama toimeainetEsimene Venemaa koroonaviiruse vastane ravim sai tervishoiuministeeriumilt heakskiiduJaapani ravimina - see tähendab 200 milligrammi favipiraviiri tableti kohta. Nagu vestluses "N + 1" -ga, millele juhtis tähelepanu RDIF-i esindaja Arseny Palagin, on vene narkootikumide täiteaine ise. Juhendis öeldakse, et abiainete hulka kuuluvad mikrokristalne tselluloos, kroskarmelloosnaatrium, kolloidne ränidioksiid, magneesiumstearaat ja povidoon K-30. Jaapani originaalse Avigani patendikaitse tähtaeg möödus 2019. aastal, seega võib seda ravimit pidada seaduslikult toodetuks. üldine.
Venemaa kliinilised uuringud Avifavir'iga pole samuti veel lõppenud. Lõpetas ainult mitmekeskuselise randomiseeritud uuringu esimese ja teise etapi, kinnitab RDIF-i vestluspartner "N + 1". Esimeses etapis osales 60 inimest - neist 20 kaasati kontrollrühma, mida raviti standardsete meetoditega. Andmeid uuritavate vanuse koosseisu ja tõsiduse kohta ei avaldatud.
Siit saate teadaRDIF ja ChemRar kontsern toimetavad juunis Venemaa haiglatesse 60 000 Avifaviiri kursust, mis on esimene Venemaa Föderatsioonis registreeritud ravim COVID-19 vastu. arendajad ise nende testide tulemuste kohta:
- uusi kõrvaltoimeid lisaks neile, mida jaapanlased aastaid tagasi registreerisid, nad ei paljastanud;
- pärast neljapäevast ravi 65 protsendil katserühma inimestest koroonaviiruse test andis negatiivse tulemuse (kontrollrühmas oli selliseid juhtumeid umbes 30 protsenti);
- kolme päeva pärast jõudis 68 protsenti katserühma inimestest normaalsele temperatuurile (kontrollis juhtus see kuuendal päeval).
Tervishoiuministeerium kiitis avifaviiri uuringute kolmanda etapi alguse heaks 1. mail 2020. Selles etapis vastavalt andmeteleRiiklik ravimiregister riikliku ravimiregistri kodulehel peab sellest osa võtma kokku 390 inimest. Samad andmed näitavad, et favipiraviiri testib veel kaks Venemaa ettevõtet: Drugs Technology (osa R-Pharm grupist) ja Promomed. Mõlemad ettevõtted alustasid katsetamist mai lõpus.
Kuigi uuringud pole lõpule viidud ja efektiivsuse kohta on teada ainult osalised andmed, lubas tervishoiuministeerium ravimit varakult registreerida - vastavalt dekreedi alusel vastu võetud kiirendatud menetluseleVenemaa Föderatsiooni valitsuse 3. aprilli 2020. aasta otsus nr 441 Vene Föderatsiooni valitsus 3. aprillil 2020 nr 441. See dekreet ütleb, et "eksamite mahu vähendamine <...>" on lubatud "tekkimise ja likvideerimise ohu tingimustes hädaolukorras».
Nii et tootja juba lubabRDIF ja ChemRar kontsern toimetavad juunis Venemaa haiglatesse 60 000 Avifaviiri kursust, mis on esimene Venemaa Föderatsioonis registreeritud ravim COVID-19 vastu. järgmise nädala lõpuks tooge haiglatesse esimesed partiid tablette.
JuhistesJuhised ravimi "Avifavir" meditsiiniliseks kasutamiseks ravimi kohta on kirjutatud, et see "valmistati piiratud hulga kliiniliste andmete põhjal ravimi kasutamise kohta ja seda täiendatakse uute andmete ilmnemisel". Kuid vastunäidustused on juba kindlaks tehtud. Nagu Jaapani Aviganil, on ka see raseduse planeerimine, Rasedus ja rinnaga toitmise periood - geneeriline ravim on samuti potentsiaalselt teratogeenne. Podagra ja hüperurikeemiaga patsiendid peaksid ravimeid kasutama ettevaatusega. Lisaks täiendati Venemaa geneeriliste ravimite vastunäidustuste loetelu ülitundlikkusega toimeaine suhtes, vanus kuni 18 aastat, raske maksa- ja neerupuudulikkus.
Apteekidesse ravimit ei toimetata: vastavalt juhistele saab ravimit kasutada ainult haiglates.
Mis on tulemus
Avifaviir on favipiraviiri geneeriline ravim, millel on selge toimemehhanism ja mis läbib kliinilisi uuringuid Venemaal ja välismaal.
Kliiniliste ajutiste uuringute tulemused näitavad, et ravim on paljulubav: väikeste puhul proovid, mida neil õnnestus kontrollida, määrata terapeutiline toime, otsustades arendajate avalduste põhjal õnnestus. Kuid kuni kliinilised uuringud on lõpule viidud ja tulemused avaldatakse eksperthinnangutes rahvusvahelistes ajakirjades, ei saa me olla täiesti kindlad, et Avifavir tõesti aitab koronaviiruse vastu haigus. Ravimi arendaja ChemRari pressiteenistus ei vastanud selle teksti avaldamise ajal N + 1 küsimustele.
Nüüd pole meil ravimeid, mis sihipäraselt ja tõhusalt SARS - CoV - 2 viiruse vastu toimiksid. Kõik selle tiitli kandidaadid on nüüd enne uue koronaviiruse ilmnemist teadaolevad ained, mis kliinilises testid (mis on just alanud) näitavad mitmete testidega pidevalt positiivset mõju piirangud. Praegu on neid kaks.
Esimene on mais esilehekülgedele jõudnud Remdesivir, ravim, mis oli mõeldud juba enne COVID-19 epideemiat teise koroonaviiruse nakkus, Lähis-Ida respiratoorne sündroom (MERS). Ameerika regulaator kiitis Remdesiviri kliinilise kasutamise heaks ametlikku lõpetamist ootamata ravimikatsetused, - stabiilse efekti olemasolu esialgsetes uuringuandmetes veenis meditsiinilist ametnikud. Seda olukorda võrreldiKõik silmad gileadil varajase registreerimisega AZTZidovudiin, esimene ravim HIV vastu.
Samal ajal ei väitnud "Remdesivir" kunagi "hõbekuuli" staatust: testid näitavadRemdesivir Covid-19 raviks - esialgne aruanneet see ei saa aidata raskete sümptomitega inimesi - kes vajavad kopsude kunstlikku ventilatsiooni, ja kergemate sümptomitega inimestele vähendab see haiguse aega nelja päeva võrra. Paljusid muid toimeid - näiteks haiguse suremuse vähenemist võrreldes teiste ravimitega - ei näidatud nendes uuringutes statistiliselt olulisena. Remdesiviri uuringute valim, millest mai lõpus teatas New England Journal of Medicine, oli 1059 inimest.
Elena Verbitskaja
Peterburi Riikliku Meditsiiniülikooli biomeditsiinistatistika osakonna juhataja akadeemik I järgi. P. Pavlova.
60 õppeainet - kas seda on palju või vähe?
Ravimi efektiivsuse testimiseks vajalike katsealuste arv arvutatakse spetsiaalsete valemite abil, mis võtavad arvesse paljusid muutujaid: näiteks indikaatorite tunnused, mida eeldatavasti võetakse arvesse, nende levik, kliiniliselt käsitletavate kontrollrühma näitajatest kõrvalekaldumise tase märkimisväärne.
Määratakse näitajad, mida testide käigus arvesse võetakse. Peamine neist on tavaliselt suremus. Hingamisteede infektsioonide korral kasutatakse integraalnäitajaid, mis võtavad arvesse näiteks palavikupäevade arvu, intensiivravi või intensiivravi osakonnas viibimise, mehaanilise ventilatsiooni ja köha päevade arvu. Kõik need teisendatakse teatud valemi järgi punktideks ja seejärel võrreldakse katserühma punkte kontrollrühma punktidega.
Mõne uurimistöö jaoks piisab 20 katsealusest. Mõne jaoks ei piisa 2000. aastast.
Enne kliiniliste uuringute algust võib väikeses rühmas läbi viia katsekatseid. Harvad pole olukorrad, kus mitmekümnest inimesest koosneva grupi jaoks avastatud mõju järgnevalt suurtes rühmades “õõnestab”.
Favipiraviiri, nagu ka Remdesiviiri, ei arendatud algselt uue koronaviiruse vastase ravimina. Ravim aastaid tagasi - nii palju, et selle patent on juba aegunud - kohandati gripi (rangelt uute viiruste, mitte hooajaliste haiguste) raviks ja seda testiti Ebola ja Zika viiruste vastu.
Jah, Venemaa teadlased näivad olevat tabanud selle kasutamise mõju ravis COVID-19 - kuid seni pole väikesel 60 inimesest koosneval valimil üksikasjalikku teavet valikumeetodite ja nende koostise kohta.
Nii et meil näivad olevat pillid. Ja veendumaks, et see on tõesti ravim, peate veidi kauem ootama.

Koroonaviirus. Nakatunud arv:
6 661 888
maailmas441 108
VenemaalLoe ka🦠
- Kui kaua immuunsus uue koronaviiruse vastu püsib?
- 6 nippi, mis tegelikult mikroobe ei peleta
- Millised võivad pandeemia uued lained välja näha

